
Médecine de Précision
en Oncologie
Nous avons la solution !

50 % des patients n’ont pas accès à une thérapie ciblée efficace car le bon test moléculaire n’a pas été réalisé.
La médecine de précision évolue très rapidement; 40 % des approbations de médicaments en oncologie au XXIème siècle sont destinées à des populations définies par des biomarqueurs, cependant :
- Dans les CBNPC, 50 % des patients n’ont pas accès à une thérapie ciblée efficace car le bon test moléculaire n’a pas été réalisé.
- Seulement 7 % des patients participent à des essais cliniques, malgré le fait que 70 % d’entre eux sont prêts à s’engager. De plus, 83 % des oncologues reconnaissent les bénéfices significatifs de ces essais pour les patients participants.
- L’accès aux tests moléculaires et à la médecine de précision est très inégal tant au niveau international mais aussi au niveau intra-territorial en raison des coûts élevés et des limitations infrastructurelles (Mateo et al., 2023).

Tendances émergentes dans le développement de médicaments

Le nombre de produits en développement en oncologie a considérablement augmenté au cours de la dernière décennie, avec plus de 2 000 produits actuellement en cours de développement.
La demande pour des populations précisément caractérisées augmente, principalement grâce aux techniques de biologie moléculaire.
La recherche et le développement en oncologie ont connu un intérêt croissant pour les médicaments ciblés, avec des mécanismes d’action innovants pour le traitement des cancers au cours de la dernière décennie.
Notre algorithme de pathologie numérique pour la caractérisation précoce des tumeurs via biologie moléculaire virtuelle prédit :
+1’000
Altérations de l’ADN et de l’ARN
21
Types de cancer
Réduction du temps
Sélection des patients les plus à risque pour des tests moléculaires d’urgence.
Suppression des tests inutiles
Réduction de moitié du nombre de tests grâce à la sélection des bons tests moléculaires.
Extension du pool de recrutement pour les essais cliniques
Identification des études cliniques les plus pertinentes à J0 pour les patients en fonction de leurs critères d’éligibilité.

Solution de recrutement
réparti & ciblé
Les CRO enregistrent leur étude dans l’interface CRO d’Ummon Crawler.
L’étude est ajoutée à notre Système d’Appariement des Essais Cliniques et distribuée aux laboratoires partenaires.
Ummon Crawler prédit les biomarqueurs moléculaires, puis génère des résultats lorsque les caractéristiques des patients correspondent à votre étude clinique.
Un rapport est envoyé au clinicien, le consentement du patient est ensuite recueilli et le contact du clinicien est envoyé au CRO.
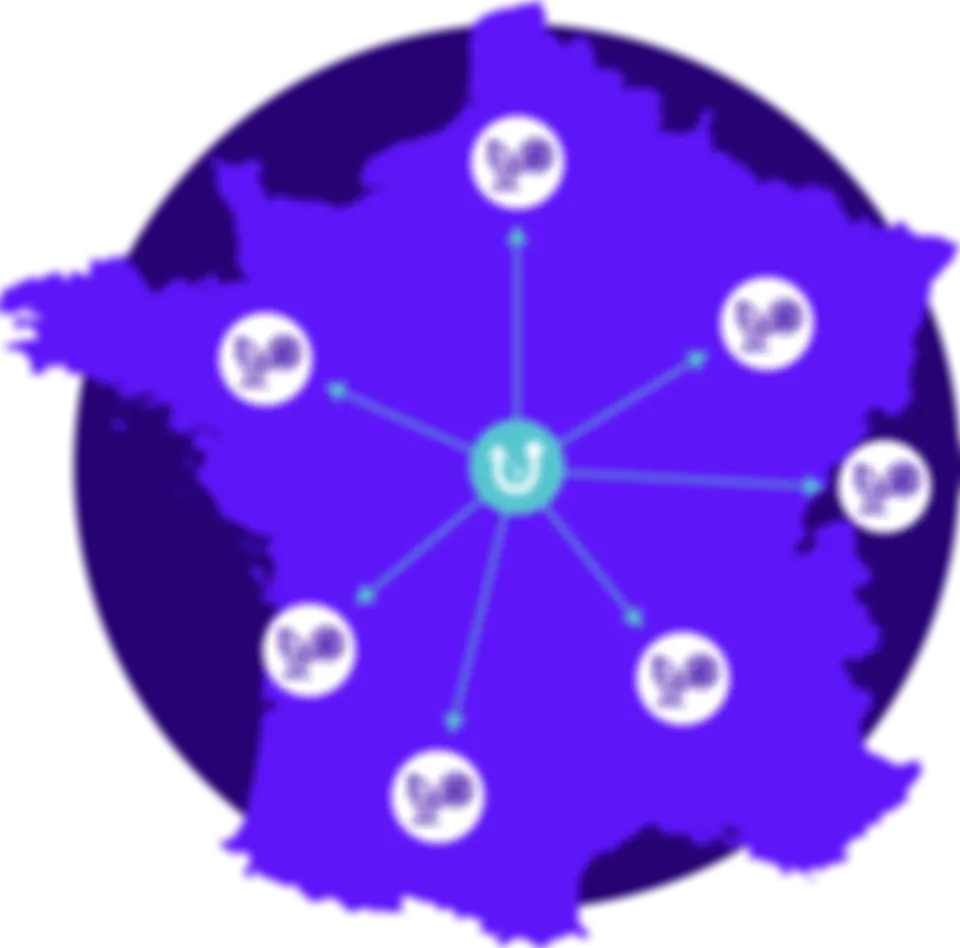
Un système d'appariement prédictif des patients

L’échantillon de tissu du patient est envoyé au pathologiste.

Chara-prAIdict prédit la biologie moléculaire à partir du tissu, et Ummon Crawler fait correspondre cela avec une vaste base de données d’essais cliniques.

Un rapport contenant les meilleures opportunités d’essais cliniques est envoyé au clinicien.

Le clinicien et le patient décident s’ils acceptent une caractérisation supplémentaire pour remplir les critères d’éligibilité, ce qui conduit à des soins de santé de référence.
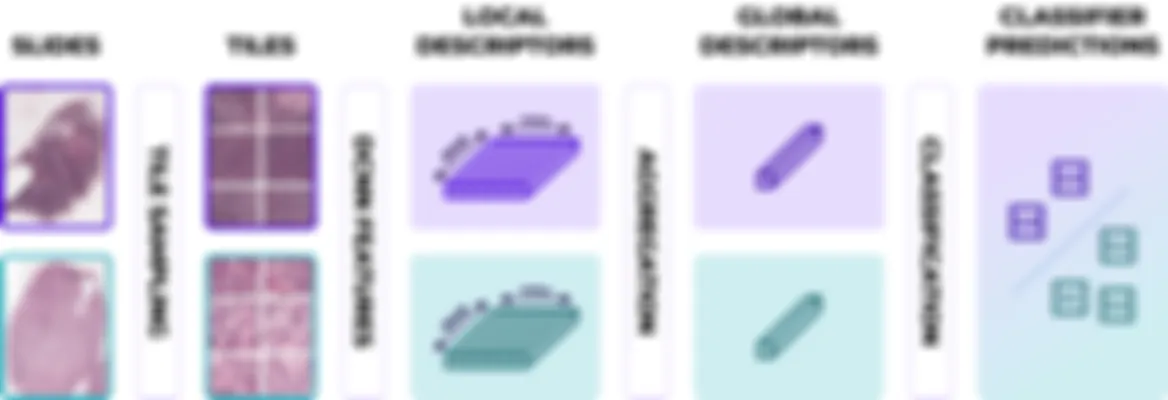
Notre Technologie
Analyse Révolutionnaire à Double Modèle
Chara-prAIdict présente un système de notation novateur qui combine le deep learning de pointe avec les informations moléculaires de la tumeur, garantissant des diagnostics de haute précision (Valderrama et al., 2024).

Calibration automatique robuste
Notre module de calibration unique surmonte les variations interlaboratoires et inter-scanners. En utilisant un processus de calibration aligné avec nos vastes bases de données, nous assurons des résultats constants et précis, renforçant ainsi la fiabilité (Dumas et al., 2022).
Expérience utilisateur intuitive
Le design ergonomique d’Chara-prAIdict permet même aux utilisateurs débutants de gérer le système en toute confiance, facilitant une analyse rapide et efficace sans compromettre la précision. Idéal pour une intégration fluide dans le flux de travail diagnostique des professionnels de la santé.

Histoire de notre Technologie
2018 - Coudray et al.
2018 - Coudray et al.
Classification et prédiction de mutation à partir d’images histopathologiques de cancer du poumon non à petites cellules à l’aide deep learning.
Nat. Med.
2020 - Fu et al.
2020 - Fu et al.
L’histopathologie computationnelle pan-cancer révèle les mutations, la composition de la tumeur et le pronostic.
Nat. Cancer
2021 - Howard et al.
2021 - Howard et al.
L’impact des signatures histologiques numériques propres à un site sur la précision et les biais des modèles de deep learning.
Nat. Commun
2021 - Van der Laak et al.
2021 - Van der Laak et al.
Deep Learning en histopathologie : le chemin vers la clinique.
Nat. Med.
2022 - Dumas et al.
2022 - Dumas et al.
Technique adversariale entre domaines sémantiques dans les images histopathologiques.
ArXiv
2023 - Morel et al.
2023 - Morel et al.
Évaluation préliminaire de deep learning pour la prédiction diagnostique de première ligne du statut mutationnel des tumeurs.
sci. rep.
2023 - Filiot et al.
2023 - Filiot et al.
Apprentissage auto-supervisé pour l’histopathologie avec modélisation d’images masquées.
sci. rep.
2024 - Valderrama et al.
2024 - Valderrama et al.
Breast-NEOprAIdict : une solution de deep learning pour prédire la réponse pathologique complète sur des biopsies de patientes atteintes de cancer du sein et traitées par chimiothérapie néoadjuvante.
In review
2024 - Morel et al.
2024 - Morel et al.
MultiVarNet : Une approche de Deep Learning et de Label Engineering pour prédire le statut mutationnel des tumeurs au niveau des protéines.
MICCAI 2024
Un positionnement unique
Pour la recherche clinique
Économique
Divisez par 3 le coût de votre stratégie de recrutement de patients.
Recrutement patient élargi
Accélérez vos études clinique en élargissant votre pool de recrutement de patients.
Pour les professionnels de la santé
Gratuit
Contrairement à la plupart des solutions de pathologie numérique (environ 25€ par clic en moyenne), ralentissant leur déploiement.
Tests additionnels pour les patients
Augmentation du nombre de tests utiles avec l’indication des panels rares actuellement non réalisés et des tests moléculaires par les fabricants souhaitant recruter des patients.
Optimisation des coûts de la sécurité social
- Avec la PCR : nous économisons 152 € par patient atteint de CBNPC.
- Avec les NGS: Notre solution permet de dépister deux fois plus de personnes pour le même nombre de tests (Morel et al., 2023).
Un moment décisif
Technologie validée
Nos pipelines d'IA ont été validés dans des revues à comité de lecture de grande qualité et dans le cadre de tests bêta.
Consortium constitué
Un consortium regroupant 20 laboratoires de pathologie, 5 partenaires des secteurs privé et public avec des homologues européens, a été créé.
Proposition sur mesure
Nous recherchons des partenaires stratégiques qui nous aideront à adapter notre processus pour améliorer leurs recrutements.
- La première étape consistera à travailler avec les laboratoires partenaires, à définir le processus, à le mettre en œuvre manuellement et à l’adapter aux besoins de chaque laboratoire.
- le mettre en œuvre manuellement, puis d’intégrer notre solution à vos offres.