
Amélioration du diagnostic tumoral
La réunion de concertation pluridisciplinaire de demain

Prédiction de la chimiosensibilité des tumeurs et du risque de rechute grâce au Deep Learning.
Notre solution révolutionne la prédiction de la réponse aux traitements et du risque de rechute, apportant une avancée considérable aux pratiques médicales actuelles.
En alliant les dernières innovations technologiques à l’analyse morphologique des tumeurs via des algorithmes de Deep Learning, nous offrons une approche performante, accessible et facilement intégrable pour un diagnostic plus précis et personnalisé. Rejoignez-nous dans la transformation de la médecine diagnostique et garantissez à chaque patient le traitement optimal dès le premier jour.

Défis actuels
L’analyse histologique reste la pierre angulaire dans le traitement du cancer, offrant une identification précise des tumeurs à travers un examen microscopique rigoureux. Ce processus est essentiel pour ajuster les traitements et assurer un suivi optimal des patients. Toutefois, les classifications morphologiques traditionnelles, comme le classement SBR ou le stade AJCC pour le cancer du sein (Valderrama et al., 2024), ne reflètent pas toujours la réponse réelle aux traitements, limitant ainsi les chances de succès thérapeutique pour certains patients.
Classical approaches
Le séquençage de nouvelle génération (NGS) et les panels de gènes, appliqués aux tumeurs ou biopsies liquides, ont transformé la prise en charge des patients atteints de cancer. Ces méthodes de pointe offrent des données précises et personnalisées pour améliorer les résultats thérapeutiques (Smith et al., 2022 ; Johnson et al., 2023). Cependant, elles négligent une dimension essentielle : l’analyse histologique des tissus. Malgré leur innovation, ces outils restent coûteux (plusieurs milliers d’euros par test), sont limités par la quantité réduite de matériel tumoral disponible, et présentent encore des défis en matière de précision et de fiabilité (Norton et al., 2023).
Solution
Prédiction de la chimiosensibilité, de la DFS (Disease Free Survival) et de l’OS (Overall Survival) à partir de l’analyse de l’histologie par IA.
Accessibilité
Réalisables à partir de l’examen de diagnostic initial.
Économique
Quelques centaines d’euros seulement.
Performant
Compléter le compte rendu médical pour offrir une médecine personnalisée de pointe dès le jour du diagnostic.
Notre Technologie
Apprentissage profond de pointe
Chemo-prAIdict combine des algorithmes propriétaires de pointe basés sur l’apprentissage profond faiblement supervisé et auto-supervisé, associés à l’apprentissage automatique traditionnel et aux voies moléculaires contextuelles, garantissant des performances et des prédictions fines pour des diagnostics de haute précision. (Valderrama et al. 2024)
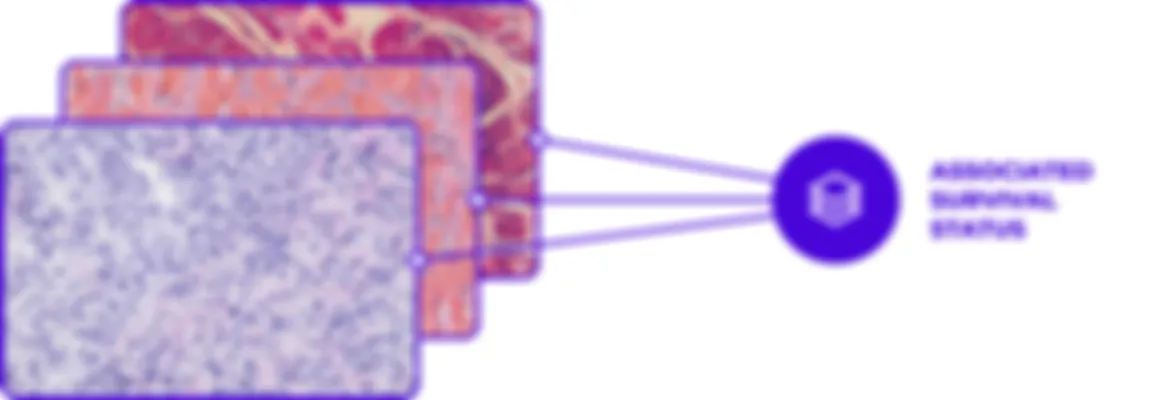
Robustesse
Nos algorithmes subissent des tests rigoureux sur des cohortes externes étendues pour garantir leur fiabilité et leur précision. Ils sont évalués pour leur cohérence biologique, ce qui implique de prédire les résultats des patients en utilisant différents échantillons pour prendre en compte l’hétérogénéité tumorale.
De plus, nos algorithmes sont évalués pour leur variabilité technique en étant testés sur différents scanners, confirmant ainsi leurs capacités à être indépendants des scanners et assurant une corrélation technique robuste. Ce processus de validation complet souligne notre engagement à fournir des solutions diagnostiques précises et cohérentes.
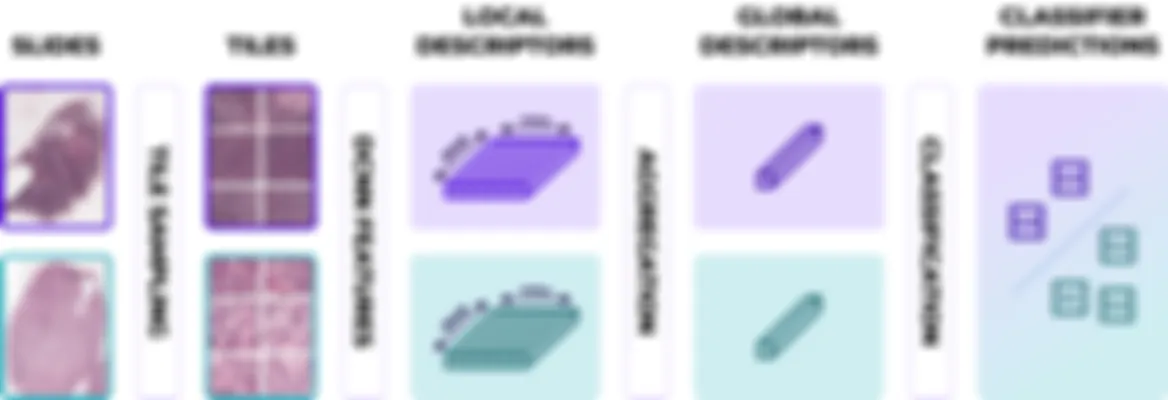
Contrôle par des experts
L’apprentissage profond fonctionne souvent comme une boîte noire, ce qui le rend difficile à contrôler et à interpréter. Pour remédier à cela, nous avons développé des méthodes automatiques d’identification des biomarqueurs qui offrent aux pathologistes une visibilité routinière de ces biomarqueurs.
Cela garantit un contrôle visuel, prévient les dérives et maintient une calibration appropriée de nos outils. Notre approche améliore la transparence et la fiabilité, facilitant des résultats diagnostiques plus précis et dignes de confiance.

Performances de notre solution sur la prédiction de la chimiosensibilité(1)
OR
1
Classification standard
Non significatif
OR
2.25-4.48
Signature génomique
(MammaPrint, OncotypeDx)(2)
OR
20.56
Chemo-prAIdict
(5-10 fois plus performants que les signatures moléculaires)
Breast-NEOprAIdict
Le premier logiciel de notre gamme Chemo-prAIdict s’intéresse à tous les cancers du sein précoces traités par chimiothérapie néoadjuvante (HER2+, HER2-/ER+, TN). Comparativement à la classification standard (moléculaire, AJCC, SBR), notre solution d’analyse de biopsie est extrêmement performante:
| Methods | OR (95% CI) | AUC | P |
|---|---|---|---|
| HER2+ | 2.70 (1.08 - 6.76) | 0.67 | 0.0358 |
| HER2-/RH+ | 20.56 (1.14-371.74) | 0.87 | 0.00413 |
| TNBC | 3.02 (1.18-7.74) | 0.71 | 0.0206 |
Nous avons pu tester notre solution sur une cohorte :
- pour les tumeurs HER2+ : 2,70 chances en plus de détecter la tumeur chimiosensible.
- pour TNBC : 3.02 chances en plus de détecter la tumeur chimiosensible.
- pour les tumeurs luminales (ER+/HER2-) : 20.56 chances en plus de détecter la tumeur chimiosensible (par rapport à la classification standard).
Ces excellents résultats font l’objet d’études complémentaires pour améliorer encore notre performance et notre niveau de preuve clinique. Nous avons également pu initier des programmes de développement dans d’autres pathologies, comme le cancer de l’ovaire et le lymphome de Hodgkin.
(1) dans le cadre des cancers du sein précoce luminaux traités par chimiothérapie néoadjuvante.
(2) Source: Freeman, J. Q. et al. Evaluation of multigene assays as predictors for response to neoadjuvant chemotherapy in early-stage breast cancer patients. npj Breast Cancer 9, 1–4 (2023)